2026年5月11日,国家药品监督管理局药品审评中心(CDE)正式发布《间充质干细胞产品药学研究与评价技术指导原则(征求意见稿)》,面向社会公开征求意见,截止日期为发布之日起一个月。这是我国首个专门针对间充质干细胞(MSC)产品的药学技术指导原则,标志着我国细胞治疗产品的监管体系正朝着更加科学、精细化的方向迈进。

一、指导原则出台的背景与核心意义
间充质干细胞因其具有自我更新、多向分化潜能以及免疫调节和组织修复等功能,在再生医学领域展现出巨大潜力。然而,MSC产品也面临来源多样、异质性强、生产工艺复杂、质量属性波动大等固有挑战,给标准化生产和质量控制带来困难。
此次CDE发布的指导原则,正是为了回应业界的迫切需求,旨在为MSC产品的研发、生产、质量研究和上市后变更提供统一、科学的技术规范。其核心意义在于,推动行业评价逻辑从过去相对粗放的“细胞符合基本表型特征”,转向真正意义上的“产品定义清晰、功能标签明确、工艺过程可控、批次质量稳定”。
二、指导原则的核心内容要点
明确产品定义与适用范围:指导原则沿用“间充质干细胞(MSC)”这一行业惯用名称,同时认可国际通用的“间充质基质细胞(MSC)”功能性术语。它主要适用于异体MSC产品(包括从人体组织分离扩增、从多能干细胞诱导分化、以及经基因修饰的功能增强型MSC),自体MSC产品及MSC来源的细胞外囊泡等可酌情参考。
引入“功能标签”核心概念:文件特别强调了“功能标签”的重要性,即反映产品疗效的可定量功能性指标集合(如免疫调节型MSC的T细胞抑制率)。这要求企业不仅关注细胞的基本表型,更要深入理解并证明产品的核心治疗功能。
构建全生命周期质量管理体系:指导原则覆盖了从生产用物料(如供者筛查、组织来源控制)、生产工艺(批次定义、工艺验证、细胞库检定)、到质量研究与稳定性考察的全链条技术要求。同时,单列章节对产品全生命周期中的关键变更(如原材料、场地、工艺、细胞库变更)提出了分级、分类的技术评价考虑,旨在建立动态、可持续的质量管理体系。
强调前瞻性技术与沟通:鼓励采用单细胞测序、多组学等新技术来深入表征细胞功能亚群,并强调了在研发过程中与监管机构进行早期沟通交流的重要性。





















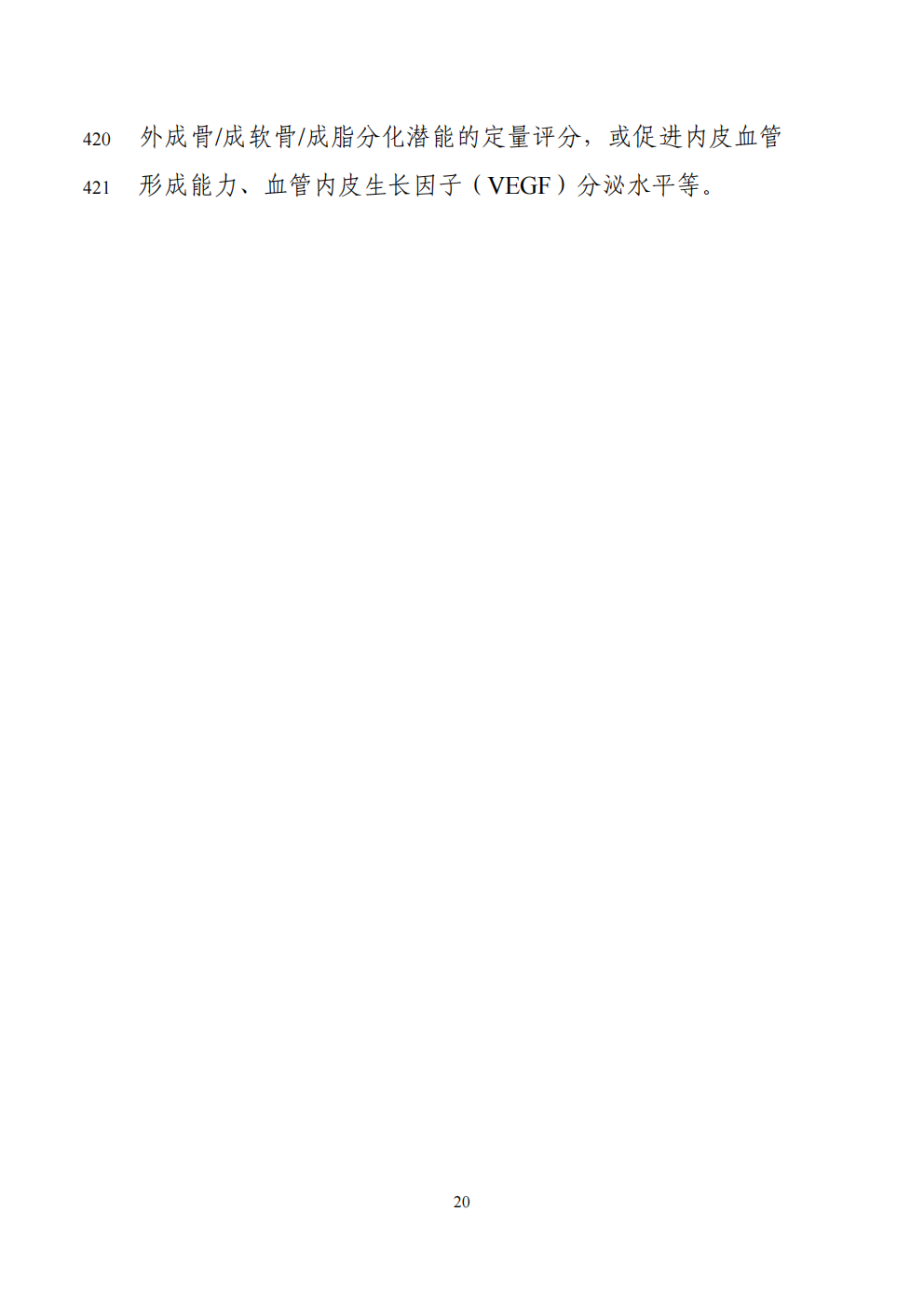
三、行业发展趋势与展望
在全球范围内,间充质干细胞赛道正进入加速发展期。数据显示,全球MSC相关市场规模持续增长,年复合增长率保持在两位数。截至近期,全球针对MSC的临床试验已超过1600项,覆盖神经退行性疾病、自身免疫疾病、组织修复等多个领域,行业发展前景广阔。
此次CDE指导原则的发布,为正处于从基础研究向规模化商业应用过渡关键阶段的国内MSC行业提供了清晰的“路标”。它意味着未来MSC产品的核心竞争力,将不只在于细胞来源或适应症故事,更在于对产品功能的深刻理解、稳定的生产工艺控制、卓越的批间一致性以及全生命周期的质量管理能力。
结语
《间充质干细胞产品药学研究与评价技术指导原则(征求意见稿)》的发布,是我国细胞治疗领域监管科学化、规范化进程中的重要一步。它不仅为研发企业指明了技术攻关和质量控制的方向,也有助于提升整个行业的产品质量水平和国际竞争力,最终让更安全、有效的创新细胞疗法惠及广大患者。
免责声明:文章仅用于科普交流,无任何商业目的不作任何商业用途,亦不表示任何医疗声明或建议。我们尊重原创,也注重分享。图文来源网络,版权归原作者所有,如涉及作品内容、版权或其它问题,请联系我们删除!


 闽公网安备 35020602002648 号
闽公网安备 35020602002648 号 QQ 客服
QQ 客服
