最近,顶级期刊《Nature Communications》上的一篇文章发现,人类的寿命极限在 120-150 岁之间,这是对来自美国、英国和俄罗斯的大量人群的健康数据进行动态评估的结果。研究发现,当人类寿命达到120至150岁时,各种身体功能的自我恢复能力达到临界值。在一个人的一生中,身体的自我修复能力开始随着年龄的增长而下降。

每个人都希望自己年迈的家人或步入老年的自己仍能参加自己喜欢的运动,与家人一起旅行……

然而,有时候往往事与愿违。随着年龄的增长,机体中出现一种促炎症反应状态进行性升高状态,这个现象命被命名为炎症性衰老。炎症性衰老(Inflammageing)与许多老年性疾病密切相关,包括心脑血管病、糖尿病、老年痴呆和癌症等。因此,抗炎或降低促炎状态成为近年来抗衰老研究的新领域。
炎症性衰老与炎症的区别
➤ 炎症性衰老的炎症特征是低度、慢性、无症状和全身性炎症。炎症老化过程的炎症属于非消退的炎症状态。
➤ 炎症通常是由面向病原体感染的宿主系统或各种类型的组织损伤引起的一系列复杂反应事件。这些事件的特征在于细胞和微环境中的因素之间的相互作用,以及生理和病理信号网络之间平衡的调节。
➤ 炎症消退:在正常情况下,当感染和组织损伤中的促炎因子被消除后,炎症反应消失(消退炎症)并保持平衡状态。
➤ 非消退炎症:体内存在不确定因素,如持续的低强度刺激和靶组织的长期过度反应,使炎症无法进入抗感染和组织损伤修复的稳定状态。相反,炎症继续发展并转变为非消退的炎症状态。
炎症性衰老与疾病的关系
炎症具有生理功能,但当炎症反应过度时,它就会变得有害,并导致许多炎症性慢性疾病,加速衰老。炎症和疾病发展之间的密切相关性是复杂的,目前尚无法阐明。
➤ 促炎与抗炎平衡:促炎细胞因子和抗炎细胞因子网络的动态平衡维持正常体内炎症的生理功能,其失衡将导致病理性变化,这是许多炎症性慢性疾病的病理基础。
➤ 因炎症衰老所致的慢性病包括如下:老年痴呆、帕金森病、动脉粥样硬化、心脏病、脑卒中、类风湿关节炎、多发性硬化症、炎症性肠炎、黄斑变性、II 型糖尿病、骨质疏松症、癌症。
此外,炎症可增加发病率和死亡率,严重损害健康。
慢性炎症中的细胞因子
在大多数人群中,慢性无菌性炎症(炎症性衰老)随着实际年龄的增长而增加。整体炎症状态不仅与个体炎症标志物的增加有关,还与各种炎症介质之间的复杂相互作用有关。
促炎标志物升高
随着年龄的增长,血液中炎症因子的水平增加,包括 IL-6、IL-8、IL-15、可溶性糖蛋白 130(SGP130,参与 IL-6 信号传导)、sCD30 和 MCP-1等。
在用于评估炎症的常见临床血清生物标志物中,CRP 和 IL-6 是研究最广泛的促炎因子。尤其是 IL-6,与衰老、身体素质差和死亡率密切相关。IL-6 可以诱导急性期蛋白(如 CRP)的产生。
IL-6 是一种影响老年人大脑、骨骼和骨骼肌的“老年因子”。IL-6 可以通过血脑屏障(BBB),也可由神经细胞释放改变神经微环境,对神经发生和神经元产生不利影响。在骨组织中,IL-6 可以影响成骨细胞和破骨细胞之间的平衡,这与骨质疏松症和溶骨性疾病有关。在骨骼肌中,IL-6 水平的释放可以发挥分解代谢作用并改变局部氧化还原平衡。IL-6 还可以通过 SASP 诱导进一步的炎症信号;因此,局部高水平的促炎细胞因子具有自我增强的能力。
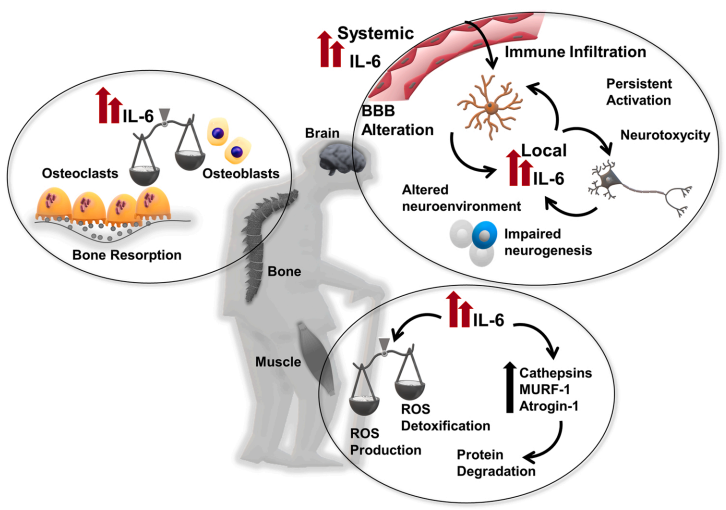
纤溶酶原激活抑制剂-1(PAI-1,也称为 SERPIN1)与 IL-6 和 CRP 属于同一促炎因子集群,PAI-1 的水平与其他衰老特征相关,包括步行速度下降和握力降低,是身体虚弱的标志。
抗炎细胞因子
抗炎因子,就其本质而言,有望减少炎症性衰老。
IL-37 是一种强大的抗炎细胞因子,确实可以抑制炎症。表达人类 IL-37 的转基因小鼠几乎没有显示出与衰老相关的促炎细胞因子的增加,并且随着年龄的增长,维持了 B 细胞祖细胞功能,恢复了 T 细胞功能,并改善了血管、代谢和运动功能。
类似地,IL-10(抗炎细胞因子)的水平与年龄增长呈负相关。IL-10 与高密度脂蛋白胆固醇一起被纳入抗炎集群,这与急性冠状动脉综合征患者的良好预后有关。
随着年龄的增长,许多抗炎因子与生理功能障碍有关。例如,sTNFR(可溶性 TNF 受体)通过阻止 TNF-α 与膜 TNFR 的相互作用,作为 TNF-α 促炎信号传导的抑制剂。因此,它们将被预期是抗炎因子,并与年龄的增长和不良身体状况呈正相关。

IL-1RA(白细胞介素-1受体拮抗剂)可以阻断 IL-1 信号传导并具有抗炎作用。然而,IL-1RA 水平与年龄呈正相关,与 IL-6 和 CRP 属于同一聚类,使其成为独立于炎症暴露或基因型的老年人死亡率的重要预测因子。
另外两种可溶性白细胞介素受体,IL-2sR(IL-2 可溶性受体)和 IL-6sR(IL-6 可溶性受体),与 TNF-α 和 sTNFRs 属于同一聚类,与较差的身体机能有关。
多种抗炎因子与衰老之间的联系,并不一定意味着这些分子是有害的,并导致炎症。相反,它们的升高可能反映了对促炎刺激的适应性生理反应,试图抑制炎症。如果高水平的抗炎因子与不良结果相关,则可能是适应性反应未能将炎症降低到破坏性阈值以下。
促炎/抗炎双重细胞因子
IL-18、TNF-α 等可以表现出抗炎和促炎双重作用,其中 IL-18 随着年龄的增长而增加,是 5 年和 10 年死亡率的独立风险预测因子。
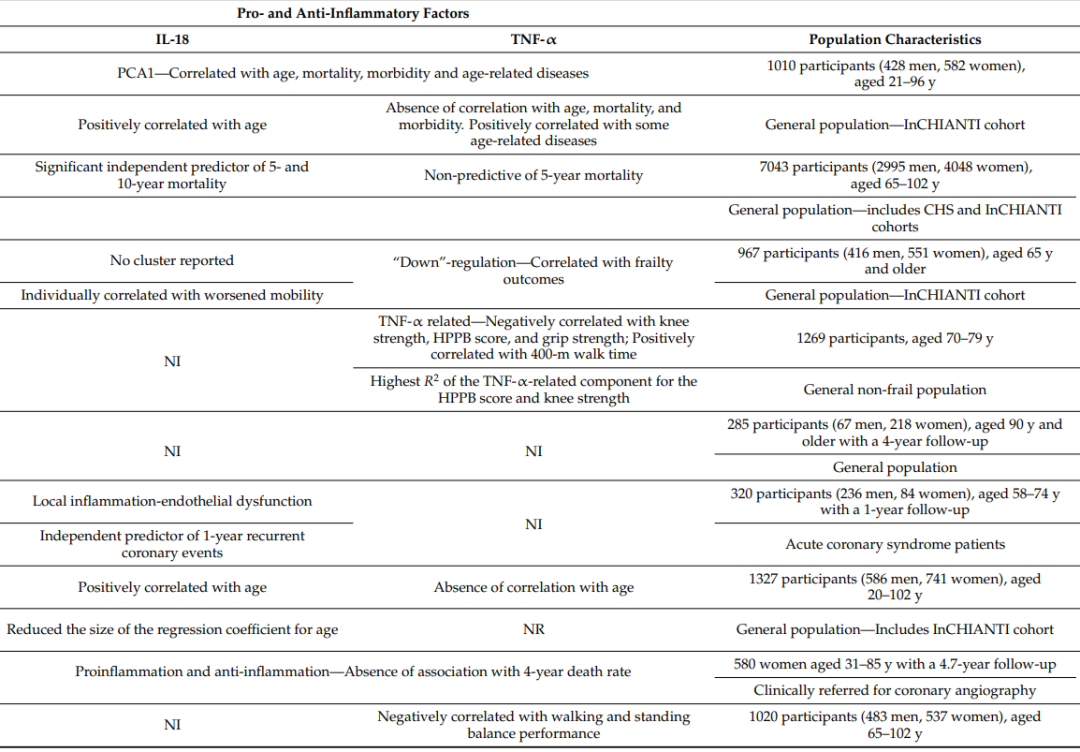
炎症性衰老与免疫衰老
炎症性衰老是由于组织免疫细胞衰老增加,以及微环境和免疫细胞的衰老相关变化,共同导致高水平的无菌性炎症,以及许多分泌性炎症因子,这些都是炎症性衰老的标志。
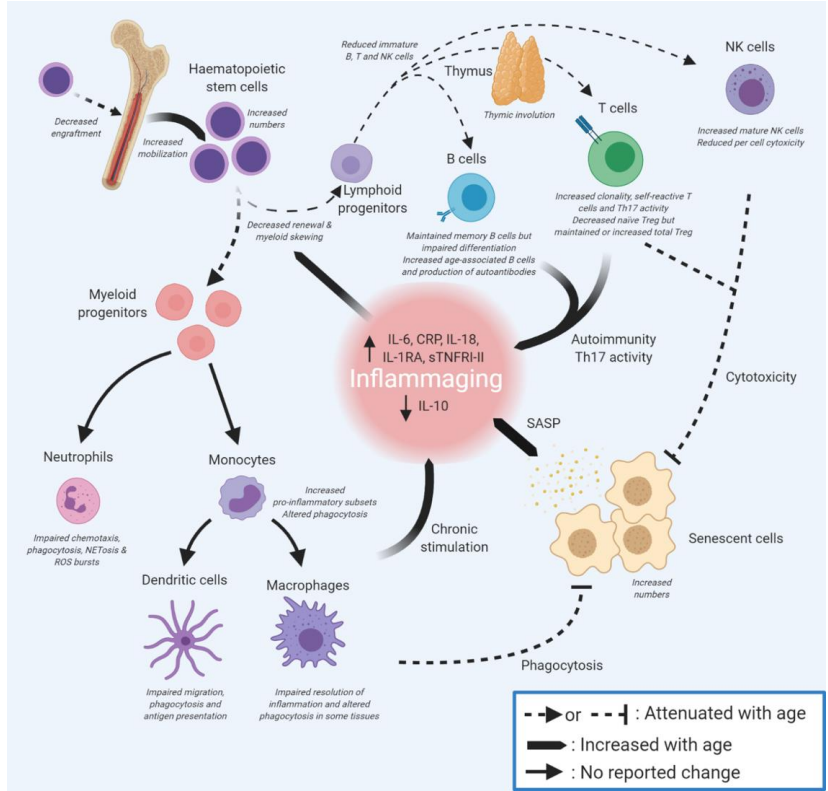
总的来说,免疫衰老和炎症性衰老是密不可分的,通过先天免疫系统和适应性免疫系统的所有组分之间的相互作用,以及通过全身衰老细胞的 SASP 产生的炎症贡献。
因此,当身体衰老时,适应性免疫细胞增加自身免疫力并促进炎症,激活促炎因子(Th17),同时免疫监测失败,无法清除衰老细胞;先天性免疫细胞驱动炎症性衰老,增加促炎亚群,并产生促炎反应。衰老的巨噬细胞可能无法从组织中清除分泌 SASP 的衰老细胞,因此,先天免疫细胞的衰老可以直接或间接促进炎症。
然而,以干细胞为核心的再生医学的发展为健康衰老提供了新的思路。此外,干细胞为延缓衰老提供了新的可能性。
近年来,干细胞抗衰老的研究引起了全球的关注。1999 年,《美国科学杂志》将干细胞的研究成果列为十大科学进步之一。经过 20 年的深入研究,干细胞治疗研究已涉及延缓衰老和治疗衰老相关疾病的方方面面。
此前,科技日报上的一篇名为《想活120岁?干细胞技术可帮你圆梦》的文章,更是让人们对干细胞与抗衰老感兴趣。
01 干细胞与抗衰老
研究表明,红骨髓被黄骨髓取代、黑发变白发都是干细胞老化和减少的表现。随着年龄增长,骨髓间充质干细胞克隆形成能力显著下降。这些研究结果揭示,衰老与干细胞老化和数量减少密切相关。
替代和修复死亡、受损细胞:干细胞具有“损伤组织趋化作用”,即干细胞会“有目的”迁移到该去的病灶处或机体细胞损伤处,替代和修复死亡、受损伤的细胞,直接起到修复损伤组织的作用。
活化体内处于休眠状态细胞:使体内干细胞数量增加,恢复早期质量,使细胞、组织器官功能年轻化,全身各系统机能得到明显改观,衰老进程得到有效的控制和缓解,机体重新焕发活力。
干细胞特具强大的分泌功能:能分泌 100 多种机体所需的细胞因子,参与血管生长、骨修复、免疫调节、造血调控、神经营养等等。改善机体各个系统的机能,提高机体免疫力等作用。
02 免疫细胞与抗衰老
免疫系统是人体抵御病原体侵犯最重要的保卫系统,由免疫器官、免疫细胞及免疫分子组成,在人体中发挥着三大功能:免疫防御、免疫监视和自身稳定。人体衰老过程中,免疫细胞的构成发生了变化:T、B 细胞绝对值明显减少,亚群也有变化,其增殖能力减弱。
免疫细胞随着衰老各种功能发生很大改变,出现对抗原的精细识别能力下降、精确调控功能减弱,以及免疫应答紊乱、低效和无效,使免疫系统的三大功能失调或减弱,最终导致癌症、感染性疾病、自身免疫性疾病的发生率明显增加。
免疫细胞能够高效识别并清除体内衰老、凋亡的细胞,对机体起着清道夫的作用,从而维持机体内环境的稳定,改善各类细胞的生存环境,减少衰老细胞的危害,直接防止衰老相关疾病的发生。
同时,免疫细胞本身可以分泌多种细胞因子,增强活化机体免疫系统,调节免疫平衡,促进身体器官新生细胞产生,提升精力体力,使机体保持年轻状态。
免疫细胞疗法通过诱导激活自体免疫细胞并回输到体内,可以提高、平衡机体免疫能力,达到有效抵抗衰老进程,消除亚健康,恢复健康状态,使与免疫相关的疾病减轻甚至治愈,减少常见病发生,甚至能够尽可能的预防癌症发生的风险。


细胞抗衰研究大大促进了人类探索抗衰老的步伐,让我们有理由相信以后人类放慢衰老的步伐将慢慢得以实现,从而实现健康老去。
免责声明:
我们尊重原创,也注重分享。图文来源网络,版权归原作者所有,如涉及作品内容、版权或其它问题,请联系我们删除!


 闽公网安备 35020602002648 号
闽公网安备 35020602002648 号 QQ 客服
QQ 客服
